O TREE
TRREE oznacza Training and Resources in Research Ethics Evaluation (Szkolenia i Dokumenty Dotyczące Oceny Etycznej Badań Biomedycznych).
TRREE to organizacja tworzona przez konsorcjum osób zarówno z krajów północy jaki i południa. Jej celem jest przygotowywanie szkoleń oraz wspieranie inicjatyw dotyczących etyki badań biomedycznych prowadzonych z udziałem ludzi, tak by spełniały najwyższe standardy i stały na straży dobrostanu osób uczestniczących w tych badaniach. TRREE osiąga te cele głównie poprzez nawiązywanie współpracy z lokalnymi współpracownikami oraz przygotowanie programu szkoleń. W początkowych etapach działalności konsorcjum TRREE było głównie zorientowane na potrzeby krajów afrykańskich.
TRREE udostępnia bezpłatny dostęp do:
- e-Learning: platforma szkolenia na odległość w zakresie etycznej oceny projektów badań naukowych umożliwiająca uzyskanie certyfikatu
- e-Resources: strony internetowej służącej do wymiany materiałów dotyczących międzynarodowych, regionalnych oraz krajowych wymagań określających zasady realizacji badań biomedycznych (przepisy prawa, standardy etyczne etc.)
Materiały szkoleniowe TRREE są obecnie dostępne w językach angielskim [EN], francuskim [FR], niemieckim [DE], polskim [PL] i portugalskim [PT].
Program szkolenia e-learning jest oparty na uznanych międzynarodowych zasadach etycznych i wymaganiach prawnych. Uwzględnia również lokalnie występujące problemy i zagadnienia prezentowane z perspektywy biednych i średnio-zamożnych krajów afrykańskich, które mają znaczenie dla osób zamierzających zapewnić ochronę uczestnikom badań naukowych oraz promować najwyższe standardy etyczne.
Ustawiczne ulepszanie programu sprzyja wymianie wiedzy, współpracy oraz wspólnemu doskonaleniu poszczególnych partnerów.
Cele
TRREE ma trzy podstawowe cele:
- Po pierwsze, szerzenie wiedzy oraz zwiększanie praktycznych umiejętności osób biorących udział w organizacji i prowadzeniu oceny etycznej badań biomedycznych oraz osób realizujących badania naukowe w ramach partnerskiej współpracy.
- Po drugie, zbudowanie opartego na współuczestnictwie procesu, który zapewni długotrwałą współpracę zarówno z jak i pomiędzy partnerami z krajów afrykańskich oraz innymi partnerami z państw biednych lub średniozamożnych.
- Po trzecie, stworzenie podstaw do swobodnego przepływu wiedzy w ramach partnerstwa krajów północy i południa. Jego celem jest zwiększanie zdolności do dokonywania oceny etycznej projektów badań biomedycznych w krajach Afryki, Europy oraz w innych państwach.
Założenia
Głównym celem modułów treningowych TRREE jest umożliwienie szkolenia oraz udostępnienie materiałów osobom, których zadaniem jest zapewnienie ochrony praw i interesów indywidualnych osób jak i całych społeczeństw, biorących udział w badaniach naukowych z zakresu ochrony zdrowia. Materiały szkoleniowe są przygotowane również z myślą o tych osobach, które współpracują podczas realizacji naukowych badań biomedycznych prowadzonych z udziałem ludzi takich jak lekarze-badacze oraz inni członkowie zespołu badawczego, studenci, członkowie komisji bioetycznych oraz pracownicy odpowiednich władz.
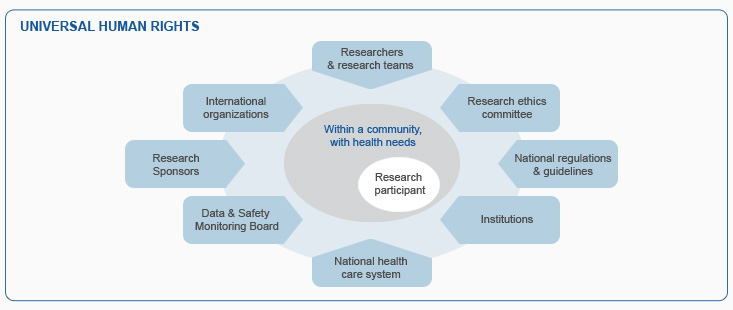
Moduły oparte są na ugruntowanych zasadach etyki badań biomedycznych, zgodnych z zapisami Deklaracji Helsińskiej. Etyka badań biomedycznych mieści się w zakresie uniwersalnych praw człowieka jak zostało to ustalone w Powszechnej Deklaracji Praw Człowieka (1948), Konwencji Praw Dziecka (1989) oraz innych międzynarodowych aktach prawnych. Badania z udziałem ludzi równie często wiążą się z ryzykiem, jak i z potencjalnymi korzyściami. Ponieważ ryzyko ponoszą głównie uczestnicy badań, dlatego ważne jest zapewnienie, że ich interesy i dobrostan będą należycie chronione. Osiągnięcie tego celu wymaga współpracy różnych stron zaangażowanych w realizację badań naukowych.
W ramach pełnionych obowiązków, na badaczach spoczywa główna odpowiedzialność za zapewnienie bezpieczeństwa i dobrostanu uczestników badań naukowych. Badacze wypełniają te zadania podczas opracowywania protokołów badań, w trakcie ich realizacji oraz pełniąc inne obowiązki. Proces etycznej oceny badań biomedycznych przez komisje bioetyczne ma również na celu zapewnienie ochrony uczestników badań. Realizacja tego celu w sposób, który jednocześnie nie ograniczy możliwości prowadzenia potencjalnie korzystnych badań biomedycznych wymaga znajomości międzynarodowych oraz lokalnych wytycznych, a także umiejętności ich analizowania.
Odbiorcy
TRREE dostarcza szkoleń oraz materiałów niezbędnych dla pracy wszystkich osób, których zadaniem jest zapewnienie ochrony interesów i dobrostanu uczestników badań naukowych oraz promowanie najwyższych standardów etycznych. Podczas gdy wybrane moduły mogą kłaść większy nacisk na kwestie istotne dla członków komisji bioetycznych lub zespołów badawczych, włączając w to badaczy, pielęgniarki czy koordynatorów badań, szkolenia są zasadniczo dostępne dla wszystkich. Ich zawartość może również zainteresować władze publiczne (a szczególnie te zajmujące się opieką zdrowotną), agencje zajmujące się oceną technologii medycznych czy refundacją, uniwersytety medyczne a także polityków, pacjentów, czy przedstawicieli mediów.
Certyfikat
Moduły 1, 2 oraz 3 zawierają pytania dołączone do materiałów szkoleniowych. Warunkiem niezbędnym, aby osoba szkoląca się mogła przejść do kolejnego etapu szkolenia jest udzielenie poprawnej odpowiedzi na pytanie.
Po zakończeniu każdego modułu osoby, które za pierwszym razem uzyskały co najmniej 70% poprawnych odpowiedzi otrzymują certyfikat.
Opłaty za uzyskanie certyfikatu Modułu GCP (Dobra Praktyka Kliniczna) dla uczestników z krajów o wysokich dochodach per capita
Filozofia działania TRREE opiera się na poszanowaniu prawa do nauki i oferowaniu bezpłatnego dostępu do modułów nauczania na odległość (e-learning). Zapewnienie ciągłego rozwoju programu oraz stałej kontroli jakości, a zwłaszcza regularnego uaktualniania jego treści wymaga wsparcia finansowego. W związku z powyższym i aby zabezpieczyć dalsze działanie i ulepszanie programu, wprowadziliśmy opłatę w wysokości 58 franków szwajcarskich (CHF) za uzyskanie oficjalnego certyfikatu ukończenia modułu 4 Dobra Praktyka Kliniczna (GCP). Opłata ta będzie pobierana tylko od uczestników z krajów o wysokich dochodach per capita (według wykazu sporządzonego w 2016 roku przez Bank Światowy). Z góry dziękujemy za zrozumienie i wsparcie, które pozwoli nam na kontynuowanie wysokiej jakości, dostosowanego do potrzeb szkoleniowych i uaktualnianego programu z zakresu etyki badań naukowych.
Dostęp do wszystkich modułów nauczania oraz pozostałych certyfikatów pozostaje bezpłatny. Płatne będzie tylko wystawienie certyfikatu dla modułu GCP.
Certyfikat wystawiony przez TRREE jest formalnie uznawany przez następujące organizacje:
 |  |
Finansowanie i współpraca
TRREE powstało jako inicjatywa akademicka, która połączyła partnerów z Afryki, Europy i Szwajcarii. Projekt został zrealizowany dzięki początkowemu finansowaniu ze strony EDCTP oraz Szwajcarskiego Narodowego Funduszu Nauki. Następnie otrzymał różne formy wsparcia finansowego od organizacji publicznych i/lub non-profit, w szczególności ze środowiska akademickiego i sektora zdrowia (logotypy i linki do naszych głównych darczyńców znajdują się na dole strony).
Prawa autorskie
© 2009, Dominique Sprumont & Clement Adebamowo, Jérôme Ateudjieu, Cédric Baume, Charles Becker, Marie-Charlotte Bouësseau, Ogobara Doumbo, Marie Hirtle, Joyce Ikingura, Wen Kilama, Dirk Lanzerath, Sébastien Lormeau, Peter Ndumbe, Alassane Niaré, Aceme Nyika, Jean-François Perret, Marcel Tanner, Douglas Wassenaar, John R. Williams
Nota prawna
Teksty ustaw oraz innych przepisów są podawane wyłącznie w celu uzasadnienia przytoczonych stwierdzeń, nie należy ich traktować, jako oficjalnych wersji tych dokumentów.
PODZIĘKOWANIA
Zespół TRREE wyraża gorące podziękowania następującym osobom za ich wsparcie i pomoc:
Pomoc administracyjna
- Dominique Mengisen (Switzerland)
- Rolf Klappert (Switzerland)
Obsługa graficzna
- Pixailes Design Graphique (Canada)
- Hughes Richartzagen (Belgium)
- Valérie Seydoux (Switzerland)
jak również wszystkim osobom, które uczestniczyły w przygotowaniu oraz ocenie tego programu szkoleniowego, a szczególnie przewodniczącym i członkom komisji bioetycznych z Mali, Kamerunu, Tanzanii i Szwajcarii.
Strona działa na platformie:
© 1999 onwards, Martin Dougiamas pod auspicjami GNU GPL.
Konsultacja IT, przygotowanie strony oraz hosting:
